So funktioniert eine E-Batterie
Unternehmen und Markt
Sekundarstufe I + II

Was ist in einer E-Batterie alles enthalten, wie ist sie aufgebaut und wie treibt sie die Motoren von Elektroautos an? Dieser Hintergrundtext erklärt die wichtigsten Punkte.
In Deutschland fahren immer mehr Elektroautos. Deren Batterien sind mit einem Smartphone-Akku vergleichbar – nur viel größer und leistungsstärker. Doch was ist in so einer Batterie alles enthalten und wie funktioniert sie überhaupt? Im Folgenden werden die wichtigsten Punkte anhand der aktuell gängigen Lithium-Ionen-Batterie erklärt.
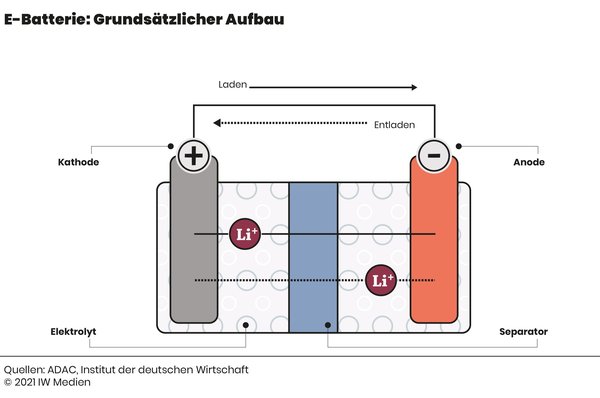
Aufbau. Auf der einen Seite der Batterie befindet sich der positive Stromableiter, der auch Kathode genannte Pluspol. Er besteht meist aus Aluminium. Das Gegenstück dazu bildet der üblicherweise aus Kupferfolie bestehende Minuspol, die Anode.
Die beiden Seiten trennt eine dünne Membran aus Kunststofffolie, der Separator. Er ist nur für die elektrisch geladenen Lithium-Moleküle, die Lithiumionen, durchlässig und verhindert so mögliche Kurzschlüsse. Eine Elektrolytlösung umgibt das Ganze und sorgt dafür, dass sich die Lithiumionen bewegen, der Strom also fließen kann.
Funktion. Wird die Batterie an eine Stromquelle angeschlossen, gibt die Kathode Elektronen ab. Sie gehen den Weg des geringsten Widerstands und fließen so über die angeschlossene Spannungsquelle zur negativen Elektrode. Entsprechend viele Lithiumionen gehen den gleichen Weg – statt über die Spannungsquelle jedoch durch den für sie durchlässigen Separator.
Wenn alle Ionen die Anode erreicht haben, ist die E-Batterie vollständig geladen.
Beim Fahren verläuft dieser Prozess genau umgekehrt und die Batterie wird entladen. Der Elektronenfluss erzeugt Strom und treibt den Motor an.
Zusammensetzung. Aktuell gibt es noch keine einheitliche Batterie für Elektroautos, auch die Lithium-Ionen-Batterien können unterschiedlich zusammengesetzt sein. Der Lithiumanteil liegt in den bisher gängigsten Hochenergie-Batterien relativ konstant bei rund 72 Gramm pro Kilo Batteriezelle, die Anteile der ebenfalls enthaltenen Metalle Nickel, Mangan und Kobalt können aber variieren.
Während die drei Materialien zunächst in gleich großen Mengen verwendet wurden, wird seit einiger Zeit verstärkt versucht, den Kobalt-Anteil zu reduzieren. Grund dafür sind die schwierigen Abbaubedingungen des Metalls.
Kobalt-Reduktion bringt Kostenvorteile
Mittlerweile hat sich der Anteil von Kobalt in einer gängigen Autobatterie von ursprünglich 200 Gramm pro Kilo Batteriezelle um fast drei Viertel auf rund 60 Gramm reduziert; hauptsächlich, indem es immer dünner auf die Elektroden aufgetragen werden konnte. Mit Mangan verhält es sich ähnlich. Um dies auszugleichen, wurde die Menge des enthaltenen Nickels parallel mehr als verdoppelt.
Das hat auch preisliche Vorteile: Während eine Tonne Kobalt derzeit rund 42.500 Dollar kostet, fallen für die gleiche Menge Nickel nur gut 18.000 Dollar an.
Dieser Text erschien zuerst auf iwd.de.